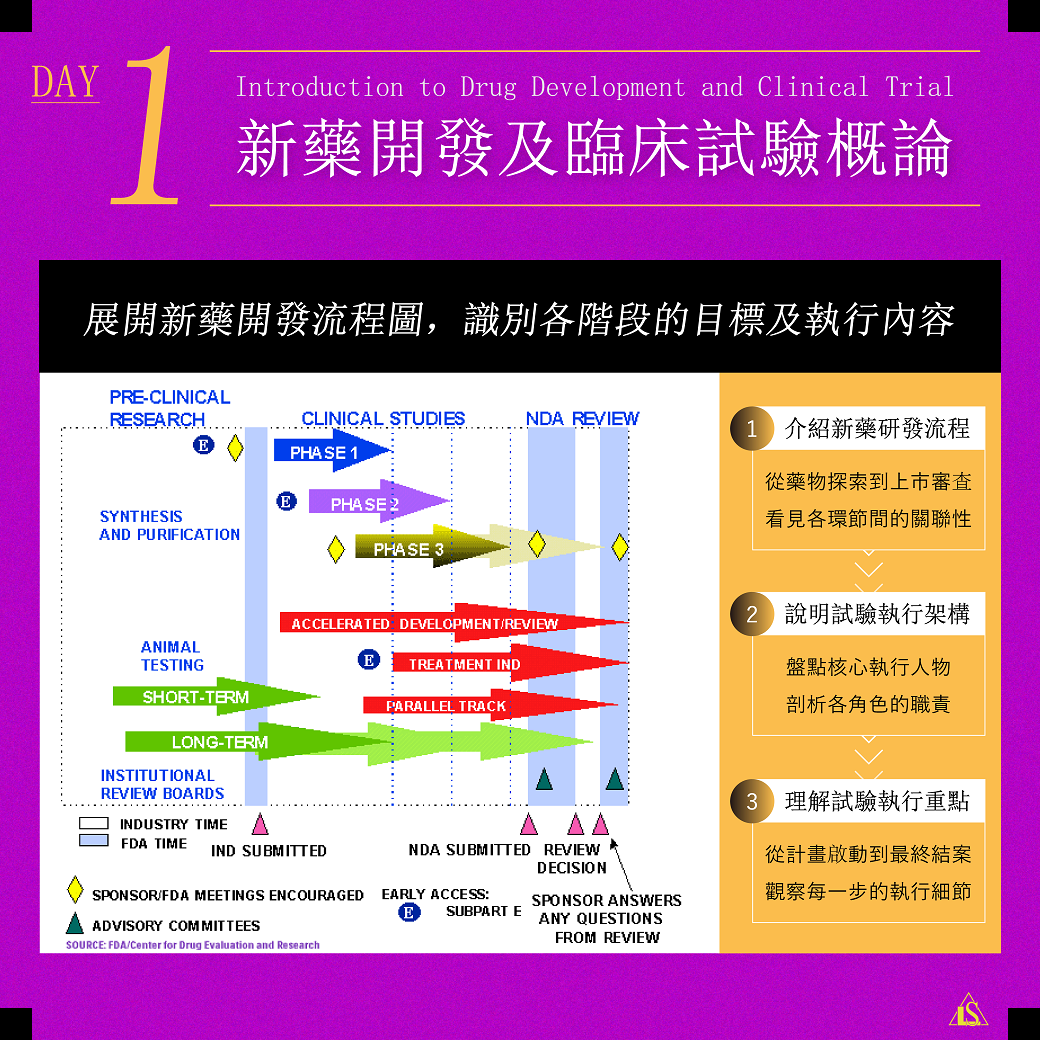
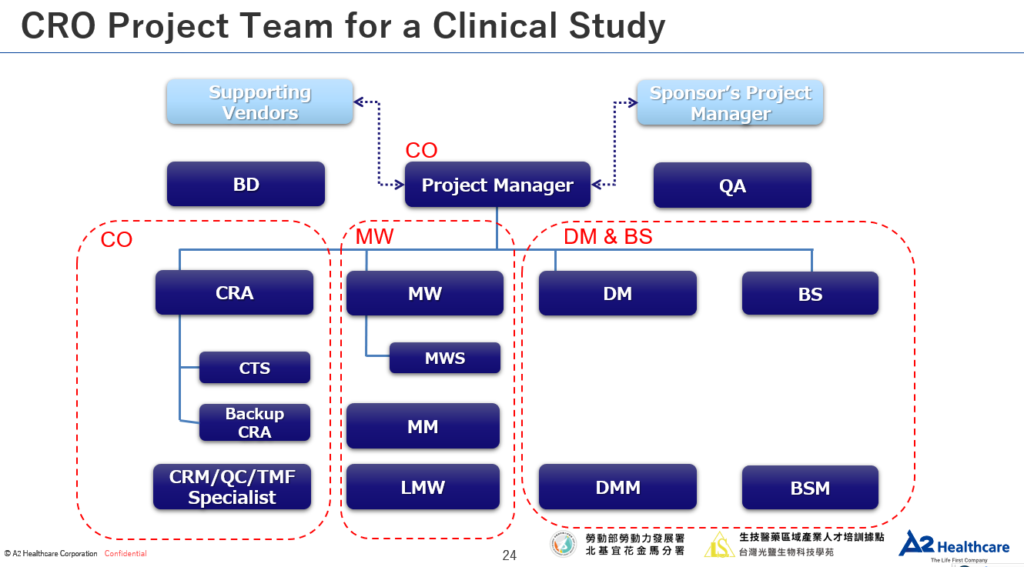
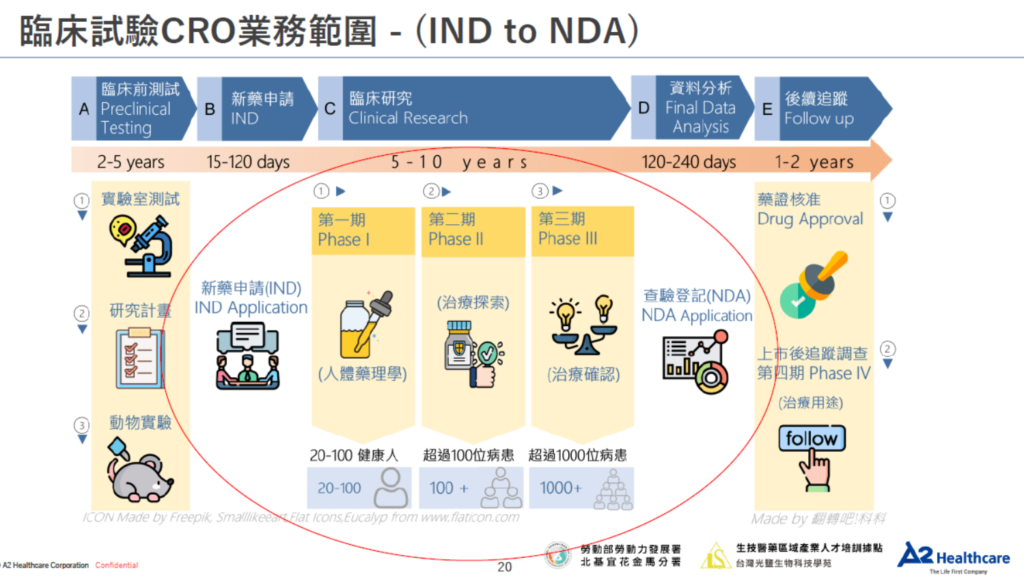
臨床試驗(Clinical trial)是新藥從研發階段通往商業化的必經之路,上市前需要先在人體內驗證其安全性及有效性,過程中牽涉到嚴謹的法規及倫理規範,唯有依賴多方團隊的協力合作下,才能順利推動新藥開發進展。
想要進入臨床試驗產業,需要具備相對應的基礎生醫背景知識,才能了解其工作內容的深意,相對的也更容易被接納。我們可以觀察到,臨床試驗從業人員多是從醫學院或生科等相關系所畢業出來的專業人士。
零經驗的新鮮人如何能快速累積對臨床試驗產業的認知?透過這堂初階概論課程,妥善利用晚上閒暇的時間,4天8小時跟隨國際CRO公司臨床試驗經理的步伐,循序漸進走過以下四大面向:臨床試驗產業環境、各團隊角色組成及分工、ICH法規依據和試驗執行流程。
根據前三屆學員的回饋,課後對臨床試驗的認識更具體了。在分工非常細的臨床試驗產業內,找到自己感興趣或不想從事的職位,對未來的工作模式及內容有更深入的了解,提供他們除了走學術研究之外的另一種職涯可能性。
關於課程
主辦單位:台灣光鹽生物科技學苑
課程地點:線上同步遠距教學 (Microsoft Teams Live Webinar)
【本線上課程未獲得講師授權,故無提供錄影檔,敬請見諒】
課程時間:114年2月17日 (ㄧ) 至2月20日 (四) 19:30至21:30 (19:00開放線上直播測試報到)
授課師資:江君敏 國際CRO公司臨床試驗經理🔎
授課內容
| 章節 | 內容 |
|---|---|
| 114/2/17 (一) 19:30至21:30 一、新藥開發及臨床試驗概論 & 臨床試驗機構執行架構及角色 | A. Introduction to Drug Development and Clinical Trial 1. 新藥臨床試驗申請 IND 2. 新藥查驗登記申請 NDA 3. 臨床試驗階段 Phases of Clinical Trials 4. 臨床試驗設計 Clinical Trial Design B. Organizational Structure of Clinical Trial Site 試驗主持人/試驗機構職責Responsibility of Investigator/Site C. Learning Check |
| 114/2/18 (二) 19:30至21:30 二、臨床試驗委託者/受託研究機構的執行架構及角色 Sponsor/CRO Organizational Structure and Professions in Clinical Trial | A. 委託者/受託研究機構 Responsibility of Sponsor/CRO 1. 臨床試驗執行 Clinical Operations 2. 資料管理 Data Management 3. 業務開發 Business Development 4. 品質管理 Quality Assurance 5. 藥品安全監視 Pharmacovigilance 6. 藥事法規 Regulatory Affairs 7. 醫藥寫作 Medical Writing 8. 醫藥事務 Medical Affairs B. Learning Check |
| 114/2/19 (三) 19:30至21:30 三、臨床試驗參與角色的規範依據 ICH-E | A. 臨床試驗規範依據ICH-E 1. 藥物主動監視 E2A-E2F 2. 臨床試驗報告 E3 3. 優良臨床試驗規範 E6 4. 臨床試驗一般考慮要點 E8 5. 臨床試驗統計 E9 B. Learning Check |
| 114/2/20 (四) 19:30至21:30 四、臨床試驗階段 & 品質管理 Phases of Clinical Trial & Quality Management | A. 臨床試驗啟動階段 Pre-trial Activities 1. 可行性評估Feasibility 2. 試驗機構評選Site Selection 3. 送審Submission 4. 監測Monitoring 5. 結案Close-out B. 品質管理 Quality Management 1. 稽核 Audit 2. 查核 Inspection 3. 根源分析及矯正預防措施 Root Cause Analysis & CAPA C. Learning Check |
課程收費&報名連結
| 一般報名 | 學生報名(檢附有效學生證或相關在學證明Email至學苑) | ||
|---|---|---|---|
| 單堂 | 系列課程(共4堂) | 單堂 | 系列課程(共4堂) |
| 800元 | 2,800元 ( | 600元 | 2,000元 ( |
* 本課程為完整系列課程,需四天全程參與 (共8小時),並完成課前/課後測驗,使得核發本線上課程結業證書
* 由於線上課程核發之電子證書需設防偽標記及建立專屬識別碼,因此將於課後兩週內連同發票寄送至您的電子信箱
歷屆學員回饋
第一屆學員心得(2020/12/7~12/11)
第二屆學員心得(2021/2/1~2/5)
第三屆學員心得(2021/4/26~4/29)
課程特色
講師介紹
江君敏
主要經歷:
- 華鼎生技顧問股份有限公司 臨床研究品管經理
- 台灣雙健維康生技顧問有限公司 品保部經理
- 健永生技股份有限公司 臨床專案經理
- 美捷國際有限公司 資深臨床研究專員
- 科文斯諮詢服務股份有限公司 資深臨床研究專員
- 台灣中外製藥股份有限公司 臨床研究專員
- 佳生科技顧問股份有限公司 臨床營運經理
相關文章
你可能感興趣?
FAQ
一、如何報名課程?
- 填寫並送出Google報名表單。
- 進入線上繳費系統完成繳費。
- 以上步驟全數完成才視為成功報名。
二、找不到繳費連結怎麼辦?
繳費連結會出現在『報名表單送出界面』。
如果你不小心關閉報名完成頁面,或是事後才想繳費,最後卻找不到繳費連結,以下提供您幾個方式:
- 重新填寫並送出報名表單,再次獲取繳費連結。
- (建議)來信學苑bioschool@biotech-edu.com索取繳費連結。
最好的方式當然是報名+繳費動作一次完成,以防時間過太久忘記繳費而錯過報名期限。
三、公司報帳要注意些什麼?
如您需報帳,可直接於線上繳費系統中輸入公司正確統編,或您可來信學苑告知。(凡發票打抬頭統編者,視為單位/公司付費派訓,結訓證書將署名「xxx單位/公司(統編公司)及學員姓名」,敬請學員自行評估,謝謝。
**特別提醒:如您需開立公司統編及抬頭,請於開課前告知,恕不接受課後進行任何形式的異動。(如有此類異動需求,也請於課前告知並說明原因。)
四、公司報名無法於線上繳費系統作業,是否有提供其他繳費管道?
公司報名作業,如無法於本繳費系統作業者,請來信或來電本學苑洽詢。我們會提供您學苑的銀行帳號,屆時再將費用匯至該帳號,並回信告知轉出帳號末五碼,如需打統編抬頭則可一併告知,使完成報名手續。
五、如何確認有報名成功?
您會在完成繳費後數個工作日內,收到由光鹽寄出的<報名成功通知信件>,收件信箱為您報名時填寫之Email。如遲遲未收到請先至『垃圾郵件』內查找,或可聯繫學苑詢問課程通知進度。
六、報名後何時可以拿到發票及證書?
如為實體課程,發票及證書將於開課日當天發放。請在離開課程會場前,確認姓名、公司抬頭統編是否正確。
如為線上課程,電子發票將於課程結束後寄送至您報名時所留的email,請於報名時確認email正確無誤。(線上課程核發之電子證書需設防偽標記及建立專屬識別碼,程序較為複雜,如有不便煩請見諒)
如您急需開立電子發票或證書,請來信或致電學苑告知原因,我們將協助加快審查程序。
七、如果還有更多問題該怎麼辦?
歡迎於上班時間 : 週一 ~ 週五 09:00 – 18:00
透過以下方式聯繫學苑
- 來信學苑信箱 bioschool@biotech-edu.com
- 致電聯繫專人客服電話 02-2545-9721
- 透過官網「聯絡我們」功能